دکتر امیرحسین حاجیمیری*: حصول اطمینان از ایجاد دسترسی به داروهای ایمن، اثربخش و مقرون بهصرفه از اصلیترین وظایف متولی سلامت در سیاستگذاری دارویی هر کشور به حساب میآید. این مفهوم اغلب با تحقق چهار A تبیین میشود.
۱.دسترسی؛
سازمان غذاودارو باید با برنامهریزی و اقدام اثربخش، برای ایجاد دسترسی به دارو در راستای آن قدم بردارد.
۲.فراهمی؛
باید زیرساخت مقتضی برای عرضه دارو در داخل مرزهای کشور برای پاسخگویی به تقاضای ایجاد شده شکل گرفته باشد. به ایجاد سهولت فیزیکی ارائه دارو در زمان و مکان مورد نیاز اشاره دارد.
۳.مقرون بهصرفهبودن؛
یک مفهوم مهم در حوزه اقتصاد سلامت، که نشان میدهد دارو بهمیزان هزینهای که ایجاد میکند از اثربخشی کافی برخوردار بوده و همچنین پرداختکننده میتواند بهطور واقعبینانه بر اساس منابع موجود برای داروهای مورد نیاز بیماران هزینه پرداخت کند.
۴.مقبولیت؛
شاخص تحقق کیفیت در عرضه دارو است که بر تمایل نظام سلامت و جامعه به مصرف یک دارو تأثیر میگذارد.
در ملاحظات پیچیده مفهوم جامع دسترسی به دارو (Access)، فهرست داروهای رسمی سازمان غذاودارو (IDL) نماد حیاتی در تحقق فراهمی محسوب شده و بهروزآوری این فهرست بهعنوان مصداقی از تعهد سازمان غذاودارو به ایجاد دسترسی رخ مینماید.
با ارزیابی دقیق داروها و افزودن آنها به فهرست رسمی، سازمان غذاودارو به تمام ذینفعان حوزه دارو در بیرون و درون نظام سلامت تضمین میدهد که این داروها تحت یک فرآیند نظاممند مورد بررسی کامل قرار گرفته و اطمینان از ایمنی، اثربخشی و هزینه-اثربخشی آنها حاصل شده است.
همانطور که در سند سیاست ملی دارویی ایران (ویرایش ۱۳۹۵) اشاره شده، سازمان غذاودارو باید از طریق تدوین روزآمد فهرست داروهای ایران تضمین نماید که بیماران به داروهایی که با استناد به منابع علمی معتبر ایمنی، اثربخشی بالینی و هزینه-اثربخش بودن آنها در درمان بیماریها ثابت شده است، دسترسی پیدا خواهند کرد.
مقاله حاضر به آخرین موارد اضافه شده به فهرست رسمی داروهای ایران در سال ۱۴۰۲ میپردازد.
اقلامی که طبق اعلام دبیر کارگروه بررسی و تدوین فهرست دارویی سازمان غذاودارو “پس از همافزایی متخصصان برای معرفی مولکولهای جدید مناسب با نیاز دارویی کشور با برگزاری ۱۷ کمیته بالینی با حضور پزشکان، متخصصان و اعضای هیأت علمی دانشگاهها در زمینههای مختلف از جمله گوارش، اورولوژی، نفرولوژی، عفونی، درد، مراقبتهای ویژه، زنان و زایمان، پوست، روماتولوژی، هماتولوژی و آنکولوژی، ریه، غدد، مغز و اعصاب و متعاقب آن ۱۷ کمیته اقتصاد دارو با متخصصان و اعضای هیأت علمی اقتصاد و مدیریت دارو به فهرست افزوده شده است”.
با نگاهی به آخرین نسخه فهرست رسمی سازمان غذاودارو که در اسفند ۱۴۰۲ از طریق پایگاه اطلاعاتی این نهاد در دسترسی عموم قرار گرفته، در سال گذشته مجموعا ۹۵ قلم داروی جدید به فهرست رسمی اضافه شده است.
در نمودار یک روند تعداد اقلام اضافه شده به فهرست طی ده سال گذشته نمایش داده شده است.
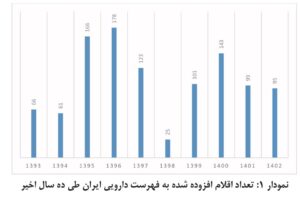
👈نمودار ۱:
تعداد اقلام افزودهشده به فهرست دارویی ایران طی ده سال اخیر
در تحلیل مقایسهای دیگر (نمودار ۲)، تعداد مولکول جدید افزوده شده در هر سال آورده شده است. در این نمودار برای مثال اگر چند قدرت از یک مولکول در لیست همان سال آورده شده باشد، یک مورد از آن در بخش آبی رنگ محسوب و سایر قدرتها در بخش نارنجی نشان داده شده است.
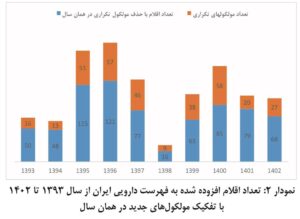
👈نمودار ۲:
تعداد اقلام افزوده شده به فهرست دارویی ایران از سال ۱۳۹۳ تا ۱۴۰۲ با تفکیک مولکولهای جدید در همان سال
در بین اقلامی که در سال ۱۴۰۲ وارد فهرست شدهاند، مولکولِ مربوط به ۴۲ قلم (۲/۴۴ درصد) قبلا در فهرست وجود داشته و به نوعی با یک شکل جدید، قدرت جدید یا تغییر سطح دسترسی وارد فهرست شده است.
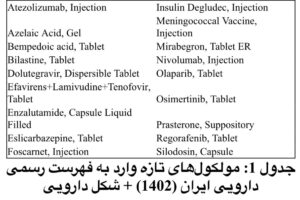
👈در جدول هم اسامی تمام مولکولهای تازه وارد فهرست رسمی داروهای ایران آورده شده است.
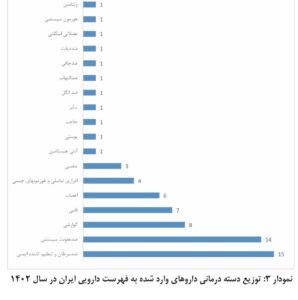
در نمودار ۳ همچنین داروهای جدید وارد شده به فهرست از حیث دستهبندی با رویکرد به تفکیک آناتومیک در ATC نشان داده شده که دسته داروهای ضدسرطان و تنظیمکننده ایمنی (L) با ۱۵ مورد در صدر قرار گرفته و به دنبال آن داروهای گوارشی (A بدون احتساب داروهای ضد دیابت) با ۱۴ و داروهای اعصاب (N) با ۶ مورد به ترتیب قابل مشاهده هستند.
از منظر سطح دسترسی نیز از میان اقلام جدید ۱۶ مورد داروی بیمارستانی، ۴ مورد داروهای معاونت بهداشت وزارت بهداشت و ۲ مورد نیز داروی OTC قابل گزارش است.
در ادامه با نگاهی به میزان جدید بودن داروهای وارد شده به فهرست در سال اخیر قابل مشاهده است که ۶ قلم از موارد، بین سالهای ۲۰۲۲ تا ۲۰۲۴ مورد تایید FDA ایالات متحده قرار گرفته است.
سال دریافت تاییدیه از FDA و نام دارو
2022👉
Atezolizumab, Insulin Degludec, Terlipressin, Trastuzumab deruxtecan
2023👉
Enzalutamide
2024👉
Osimertinib Mesylate
در نهایت لازم به تاکید است که فهرست رسمی داروهای ایران بهعنوان رکن مهم در ایجاد دسترسی دارو از منظر سیاستگذاری و همچنین نوآوری و خلق ارزش افزوده از منظر تامینکننده همواره مورد توجه بوده است.
سازمان غذاودارو مراتب بررسی و تایید هر گزینه پیشنهادی برای ورود به فهرست را با احراز مواردی نظیر داشتن تاییدیههای معتبر بینالمللی، وجود مزیت درمانی در نظام سلامت ایران و امکان عرضه با قیمتی متضمن هزینه اثربخشی به نظام دارویی کشور از مسیر کارگروه بررسی و تدوین فهرست دارویی کشور پیش میبرد.
همواره موضوعاتی متعدد در خصوص ورود به فهرست رسمی دارو بین ذینفعان در بخشهای مختلف زنجیره ارزش دارو محل بحث بوده است.
در بسیاری از موارد فرآیند ورود دارو به فهرست داروی کشور و بهتبع آن فهرست پوشش بیمهای داروها زمانبر بوده و در برخی موارد نیز بهرغم پذیرش در سطح فهرست دارویی کشور، موضوع پوشش هزینه در فهرست داروهای تحت پوشش بیمه جاری نشده است.
از سوی دیگر طی سالهای اخیر فرآیند ورود داروهای جدید به فهرست رسمی داروهای کشور در برخی شرایط نیز بهعنوان یک سد برای توسعه داروهای نوآورانه در کشور به حساب آمده است.
البته که متعاقب آن برخی ضوابط و دستورالعملها تا حدودی زیاد توانسته برخی محدودیتها را برطرف نماید.
هنوز زمانبری فرآیندهای مرتبط و همچنین محدودیت در اعطای مشوق به شرکتهای فعال در زمینه ورود داروهای جدید به فهرست، یکی از موانع قابل توجه در دسترسی به داروهای جدید تلقی میشود.
در نهایت، گزارش حاضر اشارهای به پیشرفتهای صورت گرفته در افزایش تعداد گزینههای درمانی و همچنین زمینههای بالقوه برای تحقیق و توسعه در شرکتهای دارویی ارائه نمود.
اضافه شدن هر داروی جدید به فهرست میتواند زمینه ارتقا دسترسی به مراقبتهای سلامت را فراهم آورد، لذا با مدیریت مؤثر این موضوع میتوان اطمینان حاصل کرد که این مهم به بهبود ملموس پیامدهای سلامت بیماران کشور کمک شایان خواهد کرد.
*فعال صنعت داروسازی،
متخصص اقتصاد و مدیریت دارو
/انتهای پیام/


